- Foldseek-Multimer를 통한 대규모 단백질 복합체의 구조정렬 -
[연구필요성]
생명의 분자 기계인 단백질은 복합체로 기능한다. 2024년 개발자들에게 노벨 화학상을 안긴 AlphaFold2를 통해 단백질 3차 구조(tertiary structure) 뿐만 아니라 AlphaFold-Multimer를 통해 단백질 4차 구조(quaternary structure)까지 높은 정확도로 예측할 수 있게 되었으며, 이를 통해 수백만 개의 단백질 복합체를 대규모로 예측할 수 있는 새로운 시대를 열었다. 하지만, 예측된 단백질 복합체 구조의 규모가 급격히 증가함에 따라, 기존의 정렬 도구들은 이러한 방대한 데이터를 효율적으로 분석하고 비교하는 데 한계를 보이고 있다. 이들을 빠르고 효율적으로 비교한다면 단백질 4차 구조를 생물학적 및 의학적 주요 통찰로 전환할 수 있을 것이다.
[연구성과/기대효과]
우리가 개발한 Foldseek-Multimer는 최첨단 방법보다 1,000~10,000배 빠른 속도를 자랑하며, 연구자들이 수백만 개의 단백질 복합체가 포함된 데이터베이스에서 구조적으로 유사한 4차 구조를 신속하게 식별할 수 있도록 지원한다.
이 도구는 진화적 관계 분석을 넘어, 단백질 상호작용, 대사 기능, 구조 기반 신약 개발(structure-based drug discovery) 등에 대한 새로운 통찰을 제공한다. 특히, 신약 개발 분야에서는 단백질 상호작용의 이해를 심화하고, 단백질 설계(protein design)를 가속화하며, 세포 기능에 대한 새로운 지식을 확장하는 데 기여할 것으로 기대된다.
[본문]
최근 AI 기반 단백질 구조 예측 기술, 특히 AlphaFold2의 개발로 인해 단백질 3차 구조(tertiary structure)뿐만 아니라 AlphaFold-Multimer를 통해 단백질 4차 구조(quaternary structure)까지 높은 정확도로 예측할 수 있게 되었다. 이러한 획기적인 연구 성과는 2024년 노벨 화학상으로 인정받았으며, 수백만 개의 단백질 복합체를 대규모로 예측할 수 있는 새로운 시대를 열었다. 단백질 4차 구조를 생물학적 및 의학적 주요 통찰로 전환하는 데 핵심적인 과정은 구조 정렬(structural alignment)을 통해 서로 비교하는 것이다. 하지만, 예측된 단백질 복합체 구조의 규모가 급격히 증가함에 따라, 기존의 정렬 도구들은 이러한 방대한 데이터를 효율적으로 분석하고 비교하는 데 한계를 보이고 있다.
이러한 문제를 해결하기 위해, 서울대학교 마틴 스타이네거(Martin Steinegger) 교수 연구팀은 제네바 대학교 에마뉘엘 레비(Emmanuel Levy) 교수 연구팀과 협력하여 "Foldseek-Multimer"(foldseek.com)를 개발하고 Nature Methods에 연구 결과를 발표했다. Foldseek-Multimer는 최첨단 방법보다 1,000~10,000배 빠른 속도를 자랑하며, 연구자들이 수백만 개의 단백질 복합체가 포함된 데이터베이스에서 구조적으로 유사한 4차 구조를 신속하게 식별할 수 있도록 지원한다.
Foldseek-Multimer는 단백질 복합체 구조를 대규모로 비교할 수 있는 전례 없는 속도와 민감도를 제공한다. 단백질이 복합체로 기능한다는 점을 고려할 때, 이 도구는 진화적 관계 분석을 넘어, 단백질 상호작용, 대사 기능, 구조 기반 신약 개발(structure-based drug discovery) 등에 대한 새로운 통찰을 제공한다. 특히, 신약 개발 분야에서는 단백질 상호작용의 이해를 심화하고, 단백질 설계(protein design)를 가속화하며, 세포 기능에 대한 새로운 지식을 확장하는 데 기여할 것으로 기대된다.
또한, Foldseek-Multimer는 사용자 친화적인 웹 서버(search.foldseek.com/multimer)를 통해 연구자들이 방대한 단백질 복합체 데이터를 쉽고 빠르게 검색할 수 있도록 지원한다. 압도적인 속도와 높은 정확도를 갖춘 Foldseek-Multimer는 구조 기반 단백질 복합체 분석의 필수적인 도구로 자리 잡을 전망이다. 예측된 단백질 복합체의 수가 기하급수적으로 증가하는 상황에서, Foldseek-Multimer는 연구자들이 생명체의 분자 기계(Life&s Molecular Machinery)에 대한 새로운 통찰을 얻을 수 있도록 강력한 지원을 제공할 것이다.
자세한 연구 내용은 [Nature Methods, 2025, 10.1038/s41592-025-02593-7]에서 확인할 수 있다.
[연구결과]
Rapid and Sensitive Protein Complex Alignment with Foldseek-Multimer
Woosub Kim*, Milot Mirdita, Eli Levy Karin, Cameron L.M. Gilchrist, Hugo Schweke, Johannes Söding, Emmanuel D. Levy, and Martin Steinegger
(Nature Methods in press , https://doi.org/10.1038/s41592-025-02593-7)
생명의 분자 기계인 단백질은 복합체로 기능한다. 인공지능의 발전으로 예측된 수백만 개의 단백질 복합체를 빠르고 효율적으로 비교한다면 단백질 4차 구조를 생물학적 및 의학적 주요 통찰로 전환할 수 있다. 본 연구의 결과인 Foldseek-Multimer는 최첨단 방법보다 1,000~10,000배 빠른 속도를 자랑하며, 수십억쌍의 단백질 복합체 쌍을 11시간만에 비교하였다. 이 도구는 진화적 관계 분석을 넘어, 단백질 상호작용, 대사 기능, 구조 기반 신약 개발(structure-based drug discovery) 등에 대한 새로운 통찰을 제공한다. 특히, 신약 개발 분야에서는 단백질 상호작용의 이해를 심화하고, 단백질 설계(protein design)를 가속화하며, 세포 기능에 대한 새로운 지식을 확장하는 데 기여할 것으로 기대된다.
[그림설명]
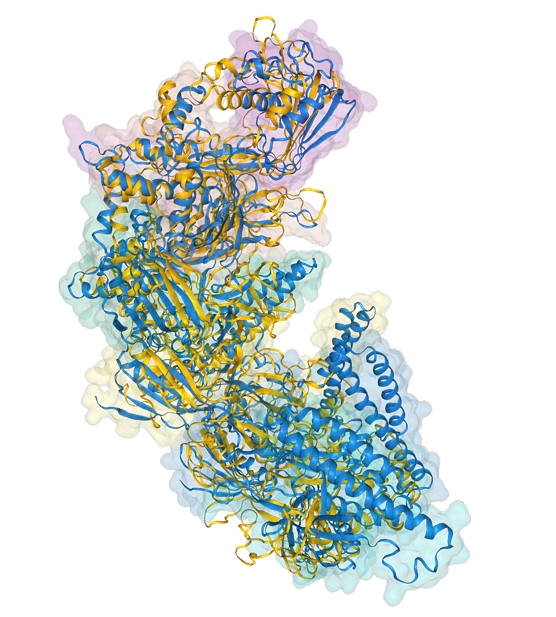
Foldseek-Multimer webserver의 단백질 복합체 비교 및 시각화의 예시.





