- 유전자적·분광학적 시그니처에 기반한 피페라진 산 함유 천연물의 발굴 및 항암 활성 규명 -
[연구필요성]
미생물 유래 천연물은 다양한 질환 치료에 필요한 약물 개발에 있어 중요한 부분을 차지한다. 신규 물질 발견을 위해서는 무작위적인 탐색이 아닌, 표적화된 논리적 발굴 방법을 이용하는 것이 시간적, 비용적 효율성을 높여준다.
[연구성과/기대효과]
본 연구에서는 유전자적·분광학적 시그니처를 이용한 피페라진 산을 포함하는 신규 물질 발굴 방법을 개발하였고, 뛰어난 항암 활성을 나타내는 신규 물질의 발견 및 생리활성 규명을 통해 선도물질로의 가능성을 제안하였다. 이러한 방법은 질소를 함유하는 다른 특이적 모핵에 대해 일반적으로 적용 가능할 것으로 예상되며, 향후 신약후보물질 발굴을 위한 천연물 개발의 중요한 기술로 사용될 것으로 기대된다.
[본문]
서울대학교 약학대학 천연물과학연구소 오동찬 교수팀과 이상국 교수팀은, 유전자적·분광학적 시그니처에 기반한 피페라진 산 함유 천연물의 표적화된 논리적 발굴 기술을 개발하였다고 보고하였다. 해당 기술을 통해 피페라진 산을 포함하는 신규 환형 펩타이드인 lenziamide A와 B를 발굴하였다. Lenziamide A는 인간 대장암 세포에 강력한 성장억제 활성을 나타내었고, 더하여 5-FU (5-fluorouracil)에 내성을 갖는 대장암 세포의 성장을 확연히 억제함을 in vitro 및 in vivo 실험 모두에서 확인하였다.
본 연구결과는 세계 최정상급 화학 학술지인 미국 화학회지 (Journal of the American Chemical Society, 피인용지수 15.0)에 ‘Targeted and Logical Discovery of Piperazic Acid-Bearing Natural Products Based on Genomic and Spectroscopic Signatures’라는 제목으로 게재되었다.
(https://doi.org/10.1021/jacs.3c04699, 공동 제1저자: 서울대학교 Daniel Shin 연구원, 변웅섭 박사, 강상욱 연구원, 교신저자: 서울대학교 오동찬 교수, 이상국 교수)
[연구 배경]
미생물 이차대사물질은 암, 병원체 감염, 대사질환, 면역조절과 같은 질병 치료를 위한 약물 개발에 있어 중요한 부분을 차지하고 있다. 과거에는 이러한 물질들의 발견이 무작위적 탐색 방법에 의존하였지만, 최근 유전자 분석기술의 발달로 생합성 유전자군의 이종 발현 및 유전자 조작 기술을 통해 신규 물질이 발굴되고 있다.
하지만 이러한 방법은 미생물의 전장 유전체가 필요하며, 수많은 미지의 생합성 유전자군에 적용이 어렵다는 단점이 있다. 다른 방법으로는 특정 생합성 유전자에 대한 PCR 스크리닝을 통해 표적 균주를 찾아내는 방법이 있다. 하지만 스크리닝 자체가 신규 물질의 발굴로 이어지기 어려우며, 표적 균주에서 표적 물질 생산 확인이 어렵다는 한계점이 있다.
[연구 결과]
본 연구에서는 유전자적·분광학적 시그니처를 활용한 피페라진 산 함유 천연물의 탐색 및 신규 물질 발굴 기술을 개발하여 앞선 한계점들을 극복하였다. 유전자적 시그니쳐를 활용하여 항암 효능 등 다양한 생리활성을 나타내는 표적 모핵인 피페라진 산을 포함하는 신규 물질 생산이 예측되는 균주를 선별하였으며, 선별된 균주 배양 추출물의 정제 전 초기 단계에서 분광학적 시그니쳐를 활용하여 표적 물질의 생산을 발견하였다. 결과적으로 이러한 표적화된 논리적 발굴 방법을 통해 신규 피페라진 산 함유 천연물을 발견하였고, 뛰어난 항암 활성을 규명하여 항암제 선도물질 발굴에 성공하였다 (그림 1).
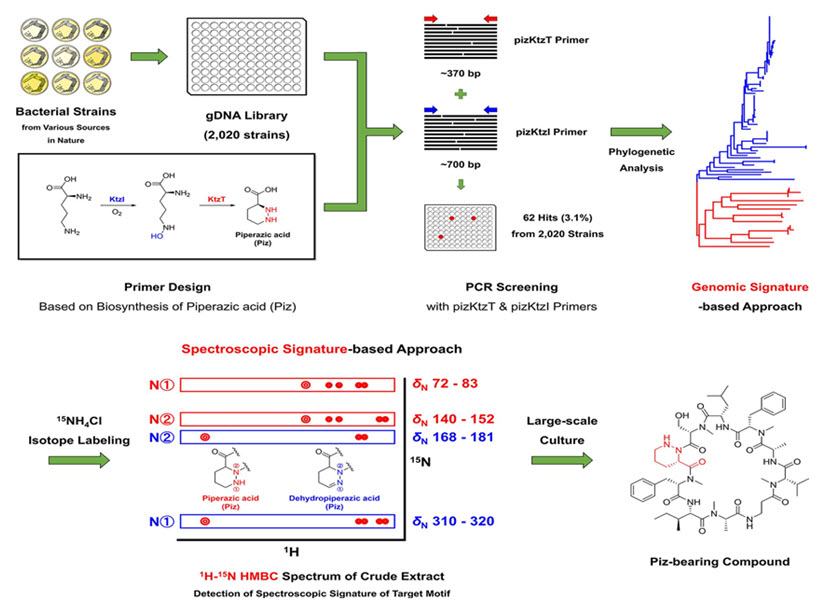
그림 1. 유전자적·분광학적 시그니쳐에 기반한 피페라진 산 함유 천연물의 발굴 과정
피페라진 산 (piperazic acid, Piz)의 생합성에는 N–N bond formation enzyme (KtzT)이라는 효소가 핵심적으로 작용한다. 본 연구에서는 해당 효소의 유전자를 시그니쳐로 활용하여 이를 표적으로 하는 PCR 프라이머를 설계 후 2,020개 균주의 DNA 라이브러리에 대해 스크리닝을 진행하였다. 그중 62개 (3.1%)의 표적 균주들을 선별하였으며, amplicon에 대한 계통분류학적 분석을 통해 계통수를 얻었다 (그림 2). 계통수는 크게 2가지의 큰 Group으로 나뉘며 총 23개의 Clade로 구성된다. 이들은 표적 균주가 생산하는 물질의 화학적 구조를 예측할 수 있도록 해주며, 이는 논리적 신규 물질 발굴 가능성을 뒷받침한다.
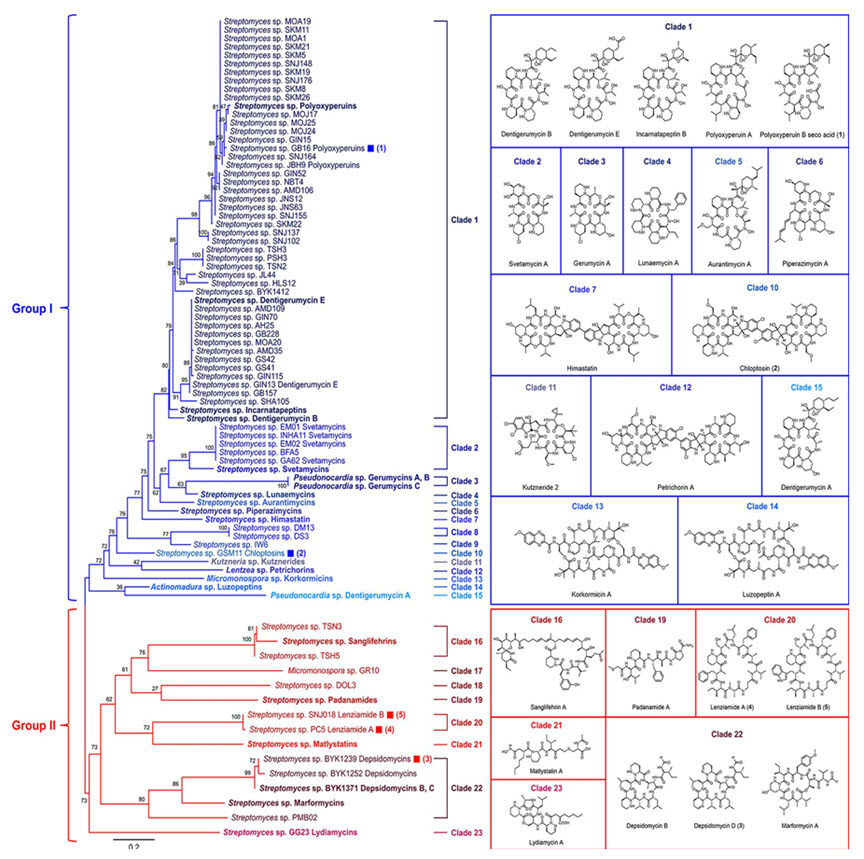
그림 . 유전자적 시그니쳐를 활용한 계통분류학적 분석
선별된 균주에 원자량 15 질소를 공급함으로써 피페라진 산 모핵의 분광학적 시그니쳐를 발견하였다. 수소와 원자량 15 질소의 2차원 핵자기공명 분광분석 (1H-15N HSQC, HSQC-TOCY, HMBC)을 통해 피페라진 산 (Piz)은 δN 72–83에서, 변형된 피페라진 산 (Dehydropiperazic acid, Dpz)은 δN 310–320에서 시그니쳐를 가짐을 규명하였다 (그림 3). 이를 활용하여 5개의 균주에서 피페라진 산 함유 신규 유도체 3가지 (Polyoxyperuin B seco acid, chloptosin, depsidomycin D)와 골격 자체가 새로운 신규 물질 2가지 (Lenziamides A, B)의 생산을 확인하였다. 이후 분광학적 분석 및 유전자 분석을 통해 각 물질의 화학적 구조를 규명하고 생합성 경로를 예측하였다.
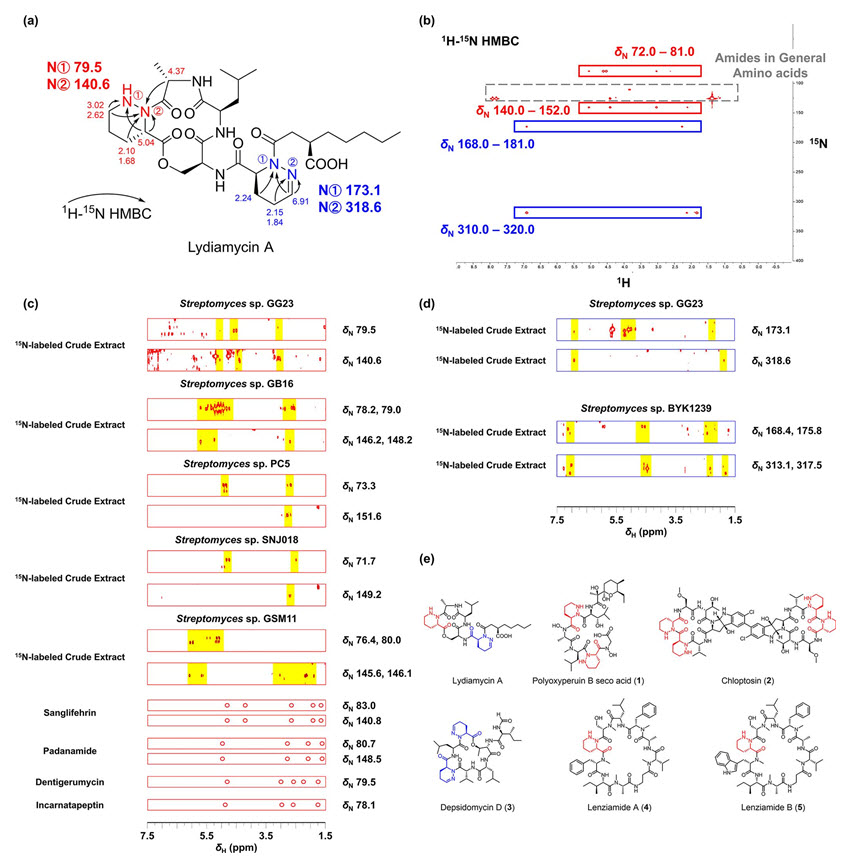
그림 3. 피페라진 산 함유 천연물의 분광학적 시그니쳐
신규 물질인 lenziamide A에 대한 생리 활성 연구 결과 항암제로서의 가능성을 확인하였다. 이는 인간 대장암 세포에 대하여 강력한 성장억제 활성을 나타내었으며, 5-FU 내성 균주에 대하여 in vitro 및 in vivo 모두에서 암세포 성장억제 활성을 나타내었다. 분자적 기전 연구 결과 lenziamide A는 STAT3의 활성화를 억제함으로써 암세포의 세포주기 정지 및 세포 자연사를 유도함을 밝혀내었다 (그림 4).
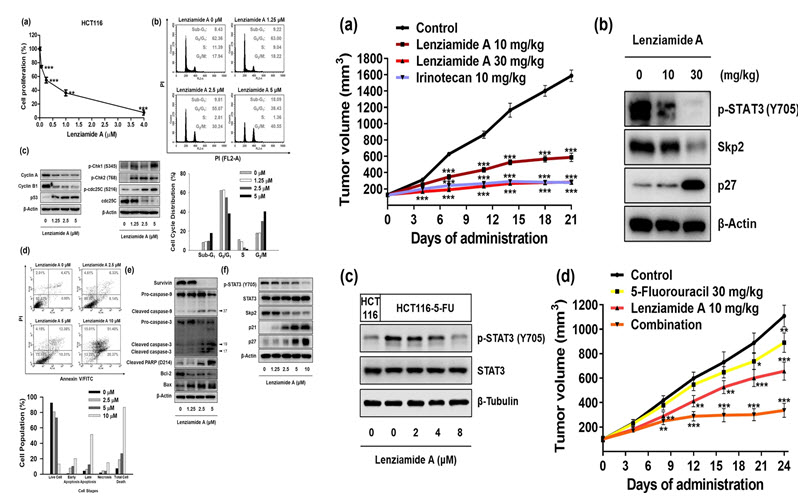
그림 4. Lenziamide A의 in vitro 및 in vivo 항암 활성 결과
[연구 결과의 의미]
미생물 유래 천연물은 다양한 질환 치료에 필요한 약물 개발에 있어 중요한 부분을 차지한다. 신규 물질 발견을 위해서는 무작위적인 탐색이 아닌, 표적화된 논리적 발굴 방법을 이용하는 것이 시간적, 비용적 효율성을 높여준다. 본 연구에서는 유전자적·분광학적 시그니쳐를 이용한 피페라진 산을 포함하는 신규 물질 발굴 방법을 개발하였고, 뛰어난 항암 활성을 나타내는 신규 물질의 발견 및 생리활성 규명을 통해 선도물질로의 가능성을 제안하였다. 이러한 방법은 질소를 함유하는 다른 특이적 모핵에 대해 일반적으로 적용 가능할 것으로 예상되며, 향후 신약후보물질 발굴을 위한 천연물 개발의 중요한 기술로 사용될 것으로 기대된다.
[기타]
본 연구는 한국연구재단 기초연구실 (BRL) 과제 및 중견연구자지원사업의 지원을 받아 수행되었다.

