서울대학교 국제농업기술대학원 염수청 교수 연구진은 ㈜ 툴젠 (대표이사:김영호) 송동우 박사 및 이화여대 이혁진 교수 연구진과 CRISPR유전자가위 mRNA를 LNP(lipid nanoparticle)로 전달하여 마우스 모델에서 혈우병 치료 타겟 유전자인 안티트롬빈(Antithrombin)을 효율적(정상의 65% 이상 회복)이고 장기적으로(10개월 이상) 조절하여 혈우병을 치료할 수 있는 연구결과를 저명한 국제학술지인 ‘사이언스 어드밴시스’ 최신호에 게재하였다.
현재 혈우병치료는 혈우병 타입별로 적합한 응고인자 단백질을 투여하는 방식이 사용된다. 하지만, 이러한 응고 단백질 제제는 반감기가 짧아 며칠에서 몇 주에 한 번씩 평생 동안 투여를 받아야 하며, 결핍한 응고인자를 단백질 치료로 보충 받을 경우 각 응고인자에 대해 inhibitor라고 부르는 항체가 생겨 치료 효과가 저해되는 경우가 많기 때문에 새로운 치료전략이 필요한 상황이다.
따라서, 현재 혈우병 치료에 있어 해결해야 할 가장 큰 2가지 이슈는 한 번의 주사로 긴 치료지속기간 제공하는 치료법 및 inhibitor를 보유한 환자들을 치료할 수 있는 방법을 찾는 것이다. Inhibitor를 보유한 환자들이 사용할 수 있는 치료제로 로슈의 Hemlibra(Emicizumab)라는 이중항체가 2017년에 승인받았는데 2021년 상반기에만 1.5조원 가까운 매출을 보이면서 혈우병 시장을 점유하고 있다. 다만 Hemlibra는 A형 혈우병 환자에만 적용될 수 있고 여전히 한 달에 한번씩 맞아야 하는 불편함이 있다. AAV를 이용한 유전자 치료 및 siRNA치료 후보들이 혈우병의 장기적 치료 또는 inhibitor를 보유한 환자 치료를 위해 개발되고 있지만 이것들을 동시에 효율적으로 해결할 수 있는 방법은 아직 임상시험에서 거의 시도되고 있지 않다.
연구팀이 수행한 연구는 기존 응고인자 단백질에 대해 inhibitor가 생겨 치료가 어려운 환자들을 포함하여 거의 모든 혈우병 환자들이 치료대상이 될 수 있는 보편적인 혈우병 치료 전략에 관한 것이다. 연구팀이 이번에 시도한 방법은 결핍된 응고인자를 직접 채워주는 기존 방식과는 달리 또 다른 응고전달통로에 관여하는 안티트롬빈 유전자를 조절하여 환자에서 트롬빈 형성을 회복시키는 일종의 우회전략(Bypassing)다. 공동연구진은 안티트롬빈 유전자에 대한 CRISPR 유전자가위 mRNA를 LNP로 전달하는 방법을 통해 혈중 안티트롬빈 양을 70%이상 감소시키고 이 효과는 최소 10개월 이상 지속되는 것을 확인하였다. 또한 두 가지 중증 혈우병 모델인 F8-인트론22역위(A형) 및 F9-녹아웃(B형) 마우스에 주입하였을 때 혈액응고 기능에 관련된 트롬빈 형성에 대한 전체적인지표들이 효율적으로 개선되는 결과를 확인하였다.
이 연구는 Bypassing전략을 통하여 inhibitor 보유 여부와 상관없이 A/B형 혈우병 환자를 대상으로 하면서도 유전자교정에 의한 안티트롬빈 저해로 장기적/영구적 효과를 기대할 수 있어 혈우병 치료의 두 가지 큰 미충적 의료수요(medical unmet needs)를 동시에 해결할 수 있는 방법으로 기대된다.
이번 연구는 한국연구재단(2017M3A9B4061406,2020R1A2C2004364), 교육부(2018R1A5A2025286), 식품의약품안전처(21173MFDS562)의 지원을 받아 수행되었다.
[연구결과]
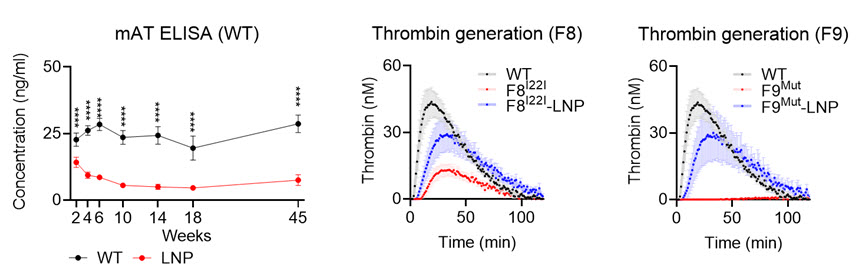
그림 1. LNP-유전자가위에 의한 혈중 안티트롬빈의 장기적인 조절 효과(왼쪽) 및 혈우병 모델(A형-가운데; B형-오른쪽)에서의 트롬빈 형성 개선 효과
- ■연구팀은 안티트롬빈 유전자에 대한 CRISPR 유전자가위 mRNA를 LNP로 전달하는 방법을 통해 혈중 안티트롬빈 양을 70%이상 감소시키고 이 효과는 최소 10개월 이상 지속되는 것을 확인하였다. 또한 두 가지 중증 혈우병 모델인 F8-인트론22역위(A형) 및 F9-녹아웃(B형) 마우스에 주입하였을 때 혈액응고 기능에 관련된 트롬빈 형성에 대한 전체적인지표들이 효율적으로 개선되는 결과를 확인하였다.
- ■또한, 유전자교정은 맞춤형질환모델 제작에도 효율적으로 사용될 수 있는데 본 연구에서도 2가지 대표적인 혈우병 모델을 자체 제작하여 치료효능을 평가하였다. 또한 임상에서도 사용될 수 있는 전달체 종류로 치료가능한 수준의 유전자교정을 확인한 의미가 크다.
- ■연구팀은 또한 수일 안에 체내에서 대사될 수 있는 LNP를 사용함으로써 필요한 시간 동안만 유전자교정 도구를 세포에 노출시키는 비교적 안전한 방법을 사용하였다. 이에 차세대 염기서열 분석(NGS) 방법을 통한 비표적(Off-target) 교정이나 항체 또는 T세포 면역반응과 관련된 분석 등을 통해 관련된 독성결과는 거의 나타나지 않음을 추가로 확인하였다.
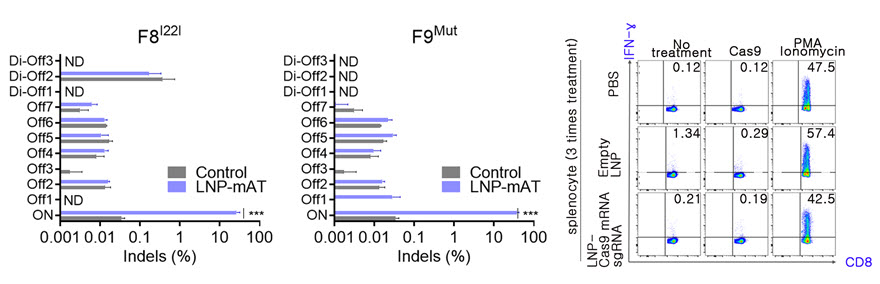
그림 2. 혈우병 모델에서(A형-왼쪽; B형-가운데) LNP-유전자가위에 의한 비표적(Off-target) 교정이 검출되지 않음. LNP-유전자가위의 반복 투여에 의해서도 낮게 유지되는 T 세포 면역반응 (오른쪽)
- ■연구팀은 “본 연구에 사용된 이온화 LNP는 기존 양이온 LNP의 낮은 전달효율과 독성을 극복할 수 있도록 자체 개발되었다. 또한 크리스퍼는 원하는 교정을 위한 시간이 많이 필요하지 않아 생체 내에서 반감기가 짧은 LNP가 바이러스 전달 체보다는 안정성 확보측면에서 더 적합 할수 있다”라고 전망했다.
- ■비슷하게 비바이러스 전달체를 이용한 유전자교정 치료제 개발 가능성은 2021년 6월 인텔리아 테라퓨틱스(Intellia Therapeutics)가 유전성 ATTR 아밀로이드증을 타겟으로 성공적으로 초기임상 결과를 발표하면서 더욱 기대되고 있는 중이다. 또한 비슷한 시기인 2021년 5월에는 버브 테라퓨틱스(Verve Therapeutics)가 염기편집(Base editing) 기술을 이용하여 고콜레스테롤혈증 치료 타겟인 PCSK9을 원숭이에서 고효율로 교정할 수 있음을 발표하기도 하였다.
- ■툴젠 김영호 대표이사는"혈우병은 유전질환 중에서도 환자수가 꽤 많아 현재도 10조 이상의 큰 시장을 형성하고 있다. 차별화된 Mode of Action으로 기존 사용되고 있는 제품들과 경쟁할 수 있도록 앞으로 진행할 비임상시험 등을 빠르게 잘 마쳐 임상에 진입할 수 있도록 노력하겠다”라고 전했다.

